Закон Шарля. Изохора
В 1787 году Ж. Шарль экспериментально установил, что при постоянном объеме давление данной массы газа прямо пропорционально температуре.
Закон Шарля При неизменном объеме V отношение давления p данной массы газа m к его абсолютной температуре T есть величина постоянная.
Термодинамический процесс, во время которого объем остается неизменным, называется изохорным (от греческих слов isos — равный и chora — занимаемое место), а линия, которая его изображает — изохорой
Математически закон Ж. Шарля можно записать в виде:
\( \dfrac
Закон Шарля может быть записан в виде:
\[ p = \dfrac
Для сравнения того же вещества при двух различных условиях, закон можно записать в виде:
\( \dfrac
Закон Шарля справедлив только для идеального газа. Он применим с определенной степенью точности к реальным газам при низких давлениях и невысоких температурах (например, атмосферный воздух, продукты сгорания в газовых двигателях и пр.)
Согласно закону Шарля изохорные процессы происходят так, что между давлением и температурой идеального газа существует линейная зависимость — при повышении температуры данной массы газа его давление возрастает.
Закон Шарля выводится как частный случай из уравнения Менделеева–Клапейрона:
\( p\cdot V = v\cdot R\cdot T \)
где R – универсальная газовая постоянная ( R = 8,31441 Дж/моль∙К ), ν – число молей вещества, P – давление газа, V – объем газа, T – температура газа.
Он может быть получен как следствие основного уравнения молекулярно-кинетической теории идеального газа:
Закон Шарля
Зако́н Ша́рля или второй закон Гей-Люссака — один из основных газовых законов, описывающий соотношение давления и температуры для идеального газа. Экспериментальным путем зависимость давления газа от температуры при постоянном объёме установлена в 1787 году Шарлем и уточнена Гей-Люссаком в 1802 году.
Содержание
Неоднозначность терминологии
В русско- и англоязычной научной литературе существуют некоторые различия в наименовании законов, связанных с именем Гей-Люссака. Эти различия представлены в следующей таблице.
| Русскоязычное название | Англоязычное название | Формула |
|---|---|---|
| Закон Гей-Люссака | Закон Шарля (en:Charles’s law) Закон Гей-Люссака Закон объёмов (Volumes Law) |  |
| Закон Шарля | Закон Гей-Люссака (en:Gay Lussac’s law) Второй закон Гей-Люссака |  |
| Закон объёмных отношений | Закон Гей-Люссака (en:Gay Lussac’s law) |
Формулировка закона
Формулировка закона Шарля следующая:
Давление газа фиксированной массы и фиксированного объёма прямо пропорционально абсолютной температуре газа.
Проще говоря, если температура газа увеличивается, то и его давление тоже увеличивается, если при этом масса и объём газа остаются неизменными.Закон имеет особенно простой математический вид, если температура измеряется по абсолютной шкале, например, в градусах Кельвина. Математически закон записывают так:
Этот закон справедлив, поскольку температура является мерой средней кинетической энергии вещества. Если кинетическая энергия газа увеличивается, его частицы сталкиваются со стенками сосуда быстрее, тем самым создавая более высокое давление.
Для сравнения того же вещества при двух различных условиях, закон можно записать в виде:
Закон Амонтона о давлении и температуре: закон давления, описанный выше, должен быть на самом деле приписан Гильому Амонтону, который в конце XVII века (точнее между 1700 и 1702 годом [1] [2] ) обнаружил, что давление фиксированной массы газа, поддерживаемого при постоянном объёме, пропорционально его температуре. Амонтон обнаружил это при постройке «воздушного термометра». Называть это закон законом Гей-Люссака просто некорректно, поскольку Гей-Люссак исследовал взаимосвязь между объёмом и температурой, а не давлением и температурой.
Закон Шарля был известен как закон Шарля и Гей-Люссака, поскольку Гей-Люссак опубликовал его в 1802 году с использованием по большей части неопубликованных с 1787 года данных Шарля. Закон Гей-Люссака, закон Шарля и закон Бойля — Мариотта все вместе образуют объединённый газовый закон. В сочетании с законом Авогадро эти три газовых закона обобщаются до уравнения состояния идеального газа.
См. также
Примечания
Ссылки
Литература
Полезное
Смотреть что такое «Закон Шарля» в других словарях:
ЗАКОН ШАРЛЯ — ЗАКОН ШАРЛЯ, объем газа при постоянном давлении прямо пропорционален его абсолютной температуре. Эта зависимость была впервые выведена Жаком ШАРЛЕМ в 1787 г. Закон представляет собой частный случай ЗАКОНА ИДЕАЛЬНОГО ГАЗА. Его иногда называют… … Научно-технический энциклопедический словарь
ЗАКОН ШАРЛЯ — один из основных газовых законов, согласно которому давление р данной массы идеального газа при постоянном объёме изменяется пропорционально изменению термодинамической (абсолютной) температуры Т: Реальные газы подчиняются этому закону при… … Большая политехническая энциклопедия
закон Шарля — Šarlio dėsnis statusas T sritis fizika atitikmenys: angl. Charles’ law vok. Charlessches Gesetz, n rus. закон Шарля, m pranc. loi de Charles, f … Fizikos terminų žodynas
Закон Бойля-Мариотта — Закон Бойля Мариотта один из основных газовых законов. Закон назван в честь ирландского физика, химика и философа Роберта Бойля (1627 1691), открывшего его в 1662, а также в честь французского физика Эдма Мариотта (1620 1684), который открыл… … Википедия
Закон Бойля — Мариотта — Воздух (или инертный газ), находящийся в запечатанном пакете с печеньем расширяется, когда продукт поднят на значительную высоту над уровнем моря (ок 2000 м) Закон Бойля Мариотта один из основных газовых з … Википедия
ЗАКОН ИДЕАЛЬНОГО ГАЗА — ЗАКОН ИДЕАЛЬНОГО ГАЗА, закон, определяющий соотношение давления, температуры и объема идеального газа: pV = nRT, где п количество молекул газа, a R универсальная ГАЗОВАЯ ПОСТОЯННАЯ; закон гласит, что при постоянной температуре (Т) произведение… … Научно-технический энциклопедический словарь
Закон Гей-Люссака — Анимация, представляющая зависимость объёма газа от температуры (закон Гей Люссака) Закон … Википедия
Шарля закон — давление pt идеального газа неизменной массы и объёма возрастает при нагревании линейно: рt = р0(1 + αt), где рt и р0 давление газа при температурах t и 0°C, α = 1/273К 1. Открыт в 1787 французским учёным Ж. Шарлем, уточнён Ж. Гей Люссаком… … Энциклопедический словарь
Закон Менделеева-Клапейрона — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнение Ван дер Ваальса Уравнение Дитеричи Разделы термодинамики Начала термодинамики Уравнен … Википедия
Закон Бойля — Воздух (или ин … Википедия
Изопроцессы в газах. Закон Шарля.
Давление р данной массы газа при постоянном объеме пропорционально температуре.
Закон Шарля был открыт французским физиком Ж. Шарлем в 1787 году.
Процесс изменения состояния термодинамической системы при постоянном объеме называется изохорным (от греч. hora — пространство).
Закон Шарля, как и другие газовые законы, является следствием уравнения состояния идеального газа:

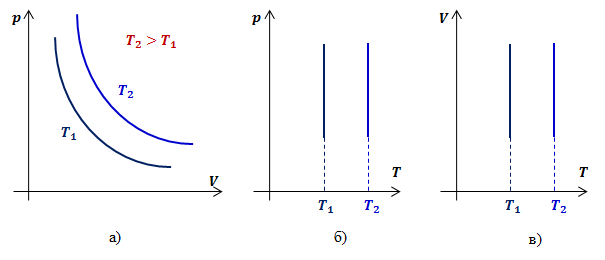
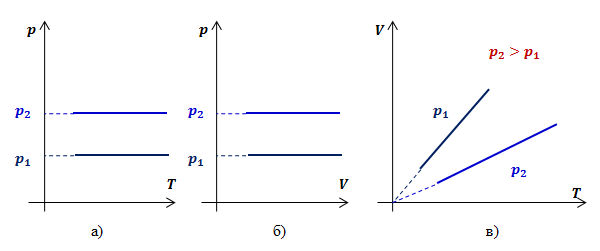
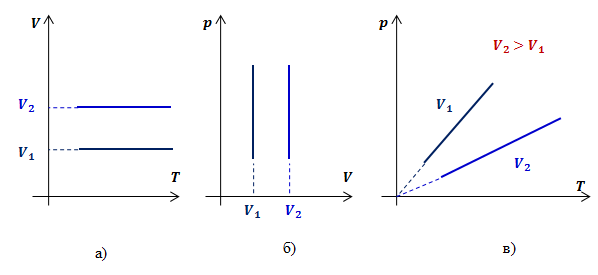
Согласно (р = const Т при V = const), давление газа линейно зависит от температуры при постоянном объеме. Эта зависимость изображается прямой, которая называется изохорой.
С ростом объема газа при постоянной температуре давление его, согласно закону Бойля-Мариотта, падает. Поэтому изохора, соответствующая большему объему, лежит ниже изохоры, соответствующей меньшему объему.
В соответствии с (р = const Т при V = const), все изохоры начинаются в точке Т = 0 (давление идеального газа при абсолютном нуле равно нулю).
Изохорный процесс используется в газовых термометрах постоянного объема.
Газовые законы
Газовые законы были открыты экспериментально, но все они могут быть получены из уравнения Менделеева-Клапейрона.
Рассмотрим каждый из них.
Закон Бойля-Мариотта (изотермический процесс)
Изотермическим процессомназывают изменение состояния газа, при котором его температура остаётся постоянной.
Для неизменной массы газа при постоянной температуре произведение давления газа на объем есть величина постоянная:
Этот же закон можно переписать в другом виде (для двух состояний идеального газа):
Этот закон следует из уравнения Менделеева – Клапейрона:
Очевидно, что при неизменной массе газа и при постоянной температуре правая часть уравнения остается постоянной величиной.
Графики зависимости параметров газа при постоянной температуре называются изотермами.
Обозначив константу буквой 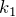
Видно, что давление газа обратно пропорционально его объему. Графиком обратной пропорциональности, а, следовательно, и графиком изотермы в координатах 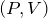
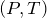
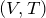
Рис.1. Графики изотермических процессов в различных координатах
Закон Гей-Люссака (изобарный процесс)
Изобарным процессомназывают изменение состояния газа, при котором его давление остаётся постоянным.
Для неизменной массы газа при постоянном давлении отношение объема газа к температуре есть величина постоянная:
Для двух состояний газа этот закон запишется в виде:
Этот закон также следует из уравнения Менделеева – Клапейрона:
Графики зависимости параметров газа при постоянном давлении называются изобарами.
Определим вид графика в координатах 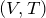
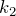
Видно, что при постоянном давлении объем газа прямо пропорционален его температуре. Графиком прямой пропорциональности, а, следовательно, и графиком изобары в координатах 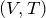
Рис.2. Графики изобарных процессов в различных координатах
Закон Шарля (изохорный процесс)
Изохорным процессомназывают изменение состояния газа, при котором его объем остаётся постоянным.
Для неизменной массы газа при постоянном объеме отношение давления газа к его температуре есть величина постоянная:
Для двух состояний газа этот закон запишется в виде:
Этот закон также можно получить из уравнения Менделеева – Клапейрона:
Графики зависимости параметров газа при постоянном давлении называются изохорами.
Для определения вида графика изохорного процесса в координатах 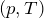
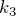
Таким образом, функциональная зависимость давления от температуры при постоянном объеме является прямой пропорциональностью, графиком такой зависимости является прямая, проходящая через начало координат (рис.3, в).
Рис.3. Графики изохорных процессов в различных координатах
Примеры решения задач
| Задание | До какой температуры нужно изобарически охладить некоторую массу газа с начальной температурой 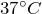 , чтобы объем газа уменьшился при этом на одну четверть? , чтобы объем газа уменьшился при этом на одну четверть? |
| Решение | Изобарный процесс 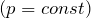 описывается законом Гей-Люссака: описывается законом Гей-Люссака: |
По условию задачи объем газа вследствие изобарного охлаждения уменьшается на одну четверть, следовательно:
откуда конечная температура газа:
Переведем единицы в систему СИ: начальная температура газа 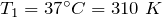
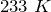 .
.| Задание | В закрытом сосуде находится газ под давлением 200 кПа. Каким станет давление газа, если температуру повысить на 30%? |
| Решение | Так как сосуд с газом закрытый, объем газа не меняется. Изохорный процесс описывается законом Шарля: |
По условию задачи температура газа повысилась на 30%, поэтому можно записать:
Подставив последнее соотношение в закон Шарля, получим:
Переведем единицы в систему СИ: начальное давление газа 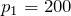
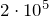
| Задание | В кислородной системе, которой оборудован самолет, имеется 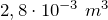 кислорода при давлении кислорода при давлении 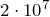 Па. При максимальной высоте подъема летчик соединяет с помощью крана эту систему с пустым баллоном объемом Па. При максимальной высоте подъема летчик соединяет с помощью крана эту систему с пустым баллоном объемом 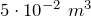 . Какое давление установится в ней? Процесс расширения газа происходит при постоянной температуре. . Какое давление установится в ней? Процесс расширения газа происходит при постоянной температуре. |
| Решение | Изотермический процесс 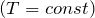 описывается законом Бойля-Мариотта: описывается законом Бойля-Мариотта: |
откуда давление, установившееся в системе:
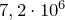 Па.
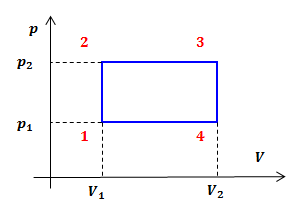
Па.| Задание | На рисунке дан график изменения состояния идеального газа в координатах 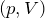 . Представить этот цикл в координатах . Представить этот цикл в координатах 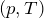 и и 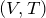 , обозначив соответствующие точки. , обозначив соответствующие точки. |
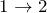 и
и 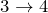 — изохоры, переходы
— изохоры, переходы 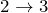 и
и 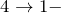 изобары.
изобары. В координатах 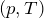
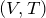
Закон шарля формула и определение график
| Законы идеальных газов |   |
| В XVII – XIX веках были сформулированы опытные законы идеальных газов. Кратко напомним их. Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным. 1. Изохорический процесс. Закон Шарля. V = const. Изохорическим процессом называется процесс, протекающий при постоянном объёме V. Поведение газа при этом изохорическом процессе подчиняется закону Шарля: При постоянном объёме и неизменных значениях массы газа и его молярной массы, отношение давления газа к его абсолютной температуре остаётся постоянным: P/Т = const. График изохорического процесса на РV-диаграмме называется изохорой. Полезно знать график изохорического процесса на РТ— и VT-диаграммах (рис. 1.6). Уравнение изохоры: Изобарическим процессом называется процесс, протекающий при постоянном давлении Р. Поведение газа при изобарическом процессе подчиняется закону Гей-Люссака: При постоянном давлении и неизменных значениях массы и газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T = const. График изобарического процесса на VT-диаграмме называется изобарой. Полезно знать графики изобарического процесса на РV— и РT-диаграммах (рис. 1.8). Изотермическим процессом называется процесс, протекающий при постоянной температуре Т. Поведение идеального газа при изотермическом процессе подчиняется закону Бойля – Мариотта: При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const. График изотермического процесса на РV-диаграмме называется изотермой. Полезно знать графики изотермического процесса на VT— и РT-диаграммах (рис. 1.10). Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой. 5. Политропический процесс. Процесс, при котором теплоёмкость газа остаётся постоянной. Политропический процесс – общий случай всех перечисленных выше процессов. 6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA=6,02·10 23 молекул (число Авогадро). 7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов: При В соответствии с законами Бойля – Мариотта (1.4.5) и Гей-Люссака (1.4.3) можно сделать заключение, что для данной массы газа Подписаться авторизуйтесь 0 комментариев Старые |





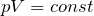
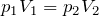
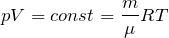
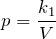
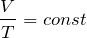
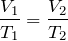
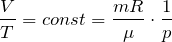
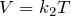
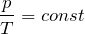
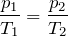
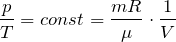
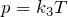
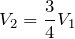
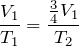
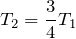
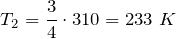
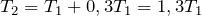
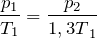
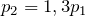
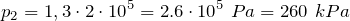
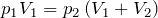
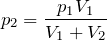
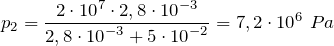

 , давление смеси газов:
, давление смеси газов: