ОПЫТ №1. Определение молярной массы диоксида углерода.



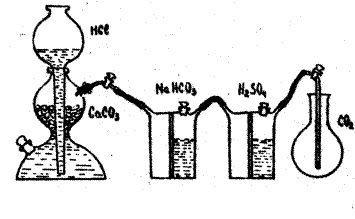
Определение молярной массы диоксида углерода проводится в приборе, состоящем из аппарата Киппа и промывных склянок (рис. 12). Диоксид углерода, получаемый в аппарате Киппа действием 10 %-й соляной кислоты на мрамор, пропускают через промывные склянки. В склянке наполненной водой СО2 очищается от примеси хлористого водорода, в склянке наполненной концентрированной серной кислотой высушивается. Для работы необходим очищенный сухой газ.
Опыт проводится в следующей последовательности: сухую и чистую колбу емкостью 250 мл плотно закрывают резиновой пробкой. Нижний уровень пробки в горле отметить карандашом для надписи по стеклу. Взвесить колбу, закрытую плотно, на электронных весах с точностью до 0,01 г.
Открыть пробку, опустить в колбу до дна газоотводную трубку от аппарата Киппа и в течение 3–5 мин. пропускать диоксид углерода с такой скоростью, чтобы можно было считать отдельные пузырьки в промывных склянках. Когда колба наполнится диоксидом углерода, вынуть газоотводную трубку, закрыть отверстие пробкой и закрыть кран аппарата Киппа. Взвесить колбу с диоксидом углерода на тех же весах.
Операцию заполнения колбы газом и последующего взвешивания повторяют 3 раза, чтобы результаты взвешивания совпадали или отличались на более чем на 0,01 г. В этом случае можно быть уверенным, что воздух в колбе вытеснен, и она полностью наполнена диоксидом углерода. Отметить показания термометра и барометра во время опыта.
Запись располагать в следующем порядке:
1. Масса колбы с пробкой и воздухом, г.
2. Масса колбы с пробкой и СО2, г.
4. Абсолютная температура во время опыта, К.
5. Атмосферное давление, мм рт. ст.
6. Объем воздуха, приведенный к нормальным условиям, мл.
7. Масса воздуха в объеме колбы, г.
8. Масса СО2 в объеме колбы, г.
9. Плотность СО2 по воздуху.
Вычислить молярную массу диоксида углерода и рассчитать процент относительной ошибки по формуле:

1. Что называется относительной плотностью газа?
2. Найти объем 20 г водорода при давлении 740 мм рт. ст. и температуре 27ºС.
3. Определите массу 80 л аммиака при давлении 780 мм рт. ст. и температуре 30ºС.
4. Вычислить молярную массу CO2, H2O и CS2.
5. Определите давление газа, если известно, что в сосуде объемом 10 л при 57ºС находится 6∙10 22 молекул.
6. Определить массу азота в баллоне, объемом в 20 л. Давление в баллоне 150 атм. (температура 20ºС).
7. При разложении бертолетовой соли выделилось 0,37 г кислорода, который при 25ºС и 750 мм рт. ст. занимал объем 300 мл. Кислород собирался под водой. Давление пара воды при 25ºС равно 23,76 мм рт. ст. Вычислить: 1) массу 1 л кислорода при нормальных условиях, 2) плотность кислорода по водороду, 3) молярную массу кислорода.
8. Определить молекулярную массу метана, если 5,6 л его при нормальных условиях весят 4 г.
9. Вычислить массу 1 м 3 азота при 30ºС и давлении 5 атм.
Определение молекулярной массы диоксида углерода
Приборы, посуда и реактивы: аппарат Киппа (с двумя промывными склянками); технохимические весы с разновесами; термометр комнатный; барометр; резиновое кольцо; сухая плоскодонная колба ёмкостью 250 мл с пробкой; мерный цилиндр на 300-500 мл; мрамор кусковой; соляная кислота (1:6); серная кислота (концентрированная); гидрокарбонат натрия (насы-щенный раствор).
Установка для получения и очистки диоксида углерода
Определить объём колбы, наполнив её водой до метки, затем измерить объём воды мерным цилиндром и записать результаты в таблицу:
| Масса колбы с воздухом и пробкой, г | Масса колбы с CO2 и пробкой, г | Объём колбы, V мл | Температура, °С | Давление, Р мм рт. ст. |
1. Объём воздуха в колбе V следует привести к нормальным
условиям (То = 273 К, Ро = 760 мм рт. ст.) по формуле:
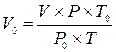
2. Вычислить массу воздуха m4, который находился в колбе, зная, что масса 1 л воздуха при нормальных условиях равна 1,29 г.
3. По разности (m1 – m4) вычислить массу пустой колбы с пробкой (m3).
4. По разности (m2 – m3) найти массу углекислого газа в колбе (m5).
6. Вычислить молекулярную массу углекислого газа (с точностью до 0,01 г):
а) по относительной плотности – M1, М1 = 29 × Dвозд;
б) по уравнению Менделеева-Клапейрона, М2, г;
в) по закону Авогадро, М3, г.
7. Определить среднюю молекулярную массу, Мср., г:
8. Определить абсолютную и относительную ошибки опыта. Составить уравнение реакции получения диоксида углерода.
Контрольные вопросы
1. Какие законы относят к основным стехиометрическим законам химии? В чем их сущность?
2. Какие величины характеризуют газовое состояние? Каковы единицы измерения массы, объёма, давления, температуры?
3. Что называется плотностью газа по воздуху? Как можно вычислить молекулярную массу вещества, зная плотность его паров по воздуху?
4. Какой вид примет формула для расчёта молекулярной массы газа, если относительную плотность его определить по азоту или по диоксиду углерода?
Дата добавления: 2015-10-21 ; просмотров: 1733 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Определение молекулярной массы диоксида углерода
Приборы, посуда и реактивы: аппарат Киппа (с двумя промывными склянками); технохимические весы с разновесами; термометр комнатный; барометр; резиновое кольцо; сухая плоскодонная колба ёмкостью 250 мл с пробкой; мерный цилиндр на 300-500 мл; мрамор кусковой; соляная кислота (1:6); серная кислота (концентрированная); гидрокарбонат натрия (насы-щенный раствор).
Установка для получения и очистки диоксида углерода
Определить объём колбы, наполнив её водой до метки, затем измерить объём воды мерным цилиндром и записать результаты в таблицу:
| Масса колбы с воздухом и пробкой, г | Масса колбы с CO2 и пробкой, г | Объём колбы, V мл | Температура, °С | Давление, Р мм рт. ст. |
1. Объём воздуха в колбе V следует привести к нормальным
условиям (То = 273 К, Ро = 760 мм рт. ст.) по формуле:
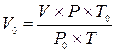
2. Вычислить массу воздуха m4, который находился в колбе, зная, что масса 1 л воздуха при нормальных условиях равна 1,29 г.
3. По разности (m1 – m4) вычислить массу пустой колбы с пробкой (m3).
4. По разности (m2 – m3) найти массу углекислого газа в колбе (m5).
6. Вычислить молекулярную массу углекислого газа (с точностью до 0,01 г):
а) по относительной плотности – M1, М1 = 29 × Dвозд;
б) по уравнению Менделеева-Клапейрона, М2, г;
в) по закону Авогадро, М3, г.
7. Определить среднюю молекулярную массу, Мср., г:
8. Определить абсолютную и относительную ошибки опыта. Составить уравнение реакции получения диоксида углерода.
Контрольные вопросы
1. Какие законы относят к основным стехиометрическим законам химии? В чем их сущность?
2. Какие величины характеризуют газовое состояние? Каковы единицы измерения массы, объёма, давления, температуры?
3. Что называется плотностью газа по воздуху? Как можно вычислить молекулярную массу вещества, зная плотность его паров по воздуху?
4. Какой вид примет формула для расчёта молекулярной массы газа, если относительную плотность его определить по азоту или по диоксиду углерода?
Дата добавления: 2014-11-13 ; просмотров: 24 ; Нарушение авторских прав
Схема установки для получения углекислого газа
ХИМИЯ
Учебно-методическое пособие
Для лабораторных работ
131000 Нефтегазовое дело
130101 Прикладная геология
 |
Лабораторная работа
«Определение молярной массы углекислого газа»
Цель работы: познакомится с методами определение молярных масс газообразных веществ (на примере углекислого газа).
1. Ознакомитесь с установкой для получения углекислого газа в аппарате Киппа и убедитесь в том, что она работает.
Аппарат Киппа- это универсальный прибор для получения газов действием жидкости на твёрдое вещество при комнатной температуре в лабораторных условиях. Изобретён голландским аптекарем Петером-Якобом Киппом в 1853 году. Состоит из трёх стеклянных сосудов; средний и нижний резервуары соединены перетяжкой, через которую проходит воронка с длинной трубкой, служащая для сообщения верхнего сосуда с нижним. Твёрдое вещество помещают в средний резервуар, снабженный газоотводной трубкой с краном. В воронку наливают жидкость, которая, заполнив нижний сосуд, поступает в средний резервуар и взаимодействует с твёрдым веществом. Выделяющийся газ выходит через газоотводную трубку. При закрытом кране газ вытесняет жидкость из среднего сосуда и реакция прекращается.
2. Колбу-приемник закройте пробкой и отметьте чертой уровень, до которого пробка вошла в горло колбы. Взвесьте на технохимических весах колбу с пробкой (mк+в).
3. Наполните колбу диоксидом углерода из аппарата Киппа, в котором протекает реакция:
Газ следует пропускать в колбу медленно, так, чтобы можно было считать пузырьки в промывных склянках.
Схема установки для получения углекислого газа
1-шарообразная воронка, 2,3- соединённые между собой резервуары, 4, 5- тубусы, 6-кран, 8 и 9- промывные склянки, 10 – приёмник углекислого газа.
4. Через 5 мин, не закрывая кран у аппарата Киппа, медленно уберите газоотводную трубку из колбы и тотчас закройте колбу пробкой.
5. Взвесьте колбу с диоксидом углерода (mк+г).
6. Измерьте рабочий объем колбы Vк, для чего наполните колбу дистиллированной водой до черты и замерьте объем воды, вылив её в мерный цилиндр.
7. Запишите значения атмосферного давления (Р) и температуры (T), при которых проводится опыт.
8. Вычислите массу воздуха (mв) в колбе по уравнению Клайперона-Менделева, на основании известной молярной массы воздуха: mв RT
10. Найдите массу пустой колбы с пробкой:
11. Найдите массу диоксида углерода в объеме колбы mг = mк+г – mк
12. Занесите все полученные значения в таблицу.
13. Вычислите молярную массу углекислого газа (Mг) двумя способами:
а) на основании плотности по воздуху:
в) по уравнению Клапейрона–Менделеева:
| mк+в | mк+г | mв | Vк | P | T | mг |
14. Вычислите среднее значение молярной массы углекислого газа (с точностью до одного знака после запятой).
15. Определите погрешность опыта, сравнивая среднее опытное значение с теоретической величиной M(CO2).
16.Сделайте выводы по проделанной работе.
Задачи для домашнего решения:
1. Установите формулу углеводорода, содержащего 81,82% углерода, масса одного литра которого при н.у. равна 1,964 г.
2. Назовите известные вам газообразные (при н.у.) вещества, которые легче и тяжелее воздуха. Рассчитайте их плотность (в г/л).
3. Какой объем займет азот массой 10 г при давлении 800 мм.рт.ст и температуре 20 о С?
Лабораторная работа
«Скорость химических реакций»
Цель работы: изучить факторы, влияющие на скорость химических реакций (на примере реакции между серной кислотой и тиосульфатом натрия).
5 Определение молярной массы диоксида углерода Лабораторная работа № 2
5 ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ДИОКСИДА УГЛЕРОДА
Лабораторная работа № 2
5.1 Цель лабораторной работы.
Определение молярной массы диоксида углерода по плотности газа и на основе уравнения Клайперона –Менделеева.
5.2 Теоретическая часть
Определение молярной масс газа может быть выполнено несколькими способами.
Определение молярной массы по плотности газа.
Плотностью одного газа по другому называется отношение масс равных объемов двух газов, измеренных при одинаковых условиях, т. е.
d = 
где d – плотность одного газа по другому;
m1 и m2 – массы равных объемов двух газов.
Поскольку в соответствии с законом Авогадро в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул, то


где М1 и М2 – молярные массы двух газов.
Сравнивая соотношения (5.1) и (5.2), получим:
d = 
Это соотношение используется для определения молярной масс газа, если известна плотность данного газа по другому (если есть возможность ее определить) и молярная масса другого газа.
Чаще всего пользуются плотностью по водороду (




где М – молярная масса исследуемого газа,
М(Н2) – молярная масса водорода, равная 2 г/моль,
М(возд.) – молярная масс воздуха, равная 29 г/моль.
Определение молярной массы газа по молярному объему.
При нормальных условиях (Т=273 К, Р= 101,3 кПа) один моль любого газа занимает объем, равный 22,4 л. Поэтому, замерив массу определенного исследуемого газа при н. у. и пересчитав на 22,4 л, получим тем самым значение его молярной массы.
Пример. Вычислить молярную массу газа, если при н. у. 0,312 г его занимают объем 0,25 л.
Ответ. Молярная масса газа равна 28,0 г/моль




где Р – давление газа, кПа;
M – молярная масса, г/моль;
R – универсальная газовая постоянная, равная 8,314 
5.3 Экспериментальная часть
5.3.1 Опыт 1.Определение молярной массы диоксида углерода
Диоксид углерода порлучается в аппарате Киппа при взаимодействии мрамора (карбонат кальция) и соляной кислоты. Написать уравнение реакции.
Чистую и сухую колбу емкостью 300-350 мл закрыть резиновой пробкой. Карандашом по стеклу отметить уровень, до которого доходит пробка в горло колбы. Колбу с пробкой взвесить на технохимических весах с точностью до 0,01 г. Записать массу колбы с воздухом (m1).
Наполнить колбу диоксидом углерода, для чего опустить в колбу до дна газоотводную трубку от аппарата Киппа и пропускать газ в течение 3-4 минут, затем, не закрывая крана, осторожно вынуть стеклянную трубку, закрыть колбу пробкой (она должна входить до метки). После этого закрыть кран аппарата Киппа (или зажим на газоотводной трубке).
Взвесить колбу с диоксидом углерода с точностью до 0,01 г, записать массу m2.
Вторично пропустить газ из аппарата Киппа в течение 2-3 минут и снова взвесить колбу. Если разница в массе при двух последних взвешиваниях не превышает 0,01 г, колба считается заполненной.
Записать температуру и атмосферное давление по барометру-анероиду (t и Р).
Измерить объем колбы, наполнив ее водой до метки. Воду из колбы вылить в мерный цилиндр, объем воды равен объему диоксида углерода. Записать эту величину (V).
А) Масса диоксида углерода в колбе (

где mв – масса воздуха, которым была заполнена колба.
Величины m1 и m2 определены экспериментально. Массу воздуха (mв) нужно подсчитать по уравнению Клайперона-Менделеева:



Вычислить массу диоксида углерода (
В) Вычислить мольную массу диоксида углерода по уравнению Клайперона-Менделеева:

С) Подсчитать относительную ошибку опыта:
П =
5.4 Контрольные вопросы и задачи
1 Что называется относительной молекулярной массой вещества? В каких единицах она измеряется?
3 Что называется молярной массой вещества? В каких единицах она измеряется?
4 Что называется относительной плотностью одного газа по другому?
5 Методы определения молярной массы газов и паров.
6 Плотность газа по кислороду равна 2. Вычислить молярную массу этого газа.
7 Масса 0,5 л газа при н. у. равна 1,58 г. Вычислить плотность этого газа по водороду.
8 Какой объем при н. у. займут: а) 17 г аммиака; б) 17 г сероводорода.
9 2 г диоксида серы при 230С занимают объем 500 мл. Под каким давлением находится газ?